こちらの記事では、「E2B(R3)実装ガイドに対応した市販後副作用等報告及び治験副作用等報告に関するQ&Aの改正について」例示を用いて説明します。
分かりやすい言葉で説明します。
筆者情報
製薬業界12年以上勤務をしており、今は管理職に就いています。
小さな会社なので、守備範囲も広く、毎日新しいことにチャレンジしてながら、フルタイムで働き2歳と4歳の子育てをしています。
解説する通知
令和2年12月9日
事務連絡
「E2B(R3)実装ガイドに対応した市販後副作用等報告及び 治験副作用等報告に関する Q&A の改正について 」
・医薬品副作用全ての通知はこちらのPMDAサイトからチェック可
副作用等の報告に関する情報
表の見方
【市販後】:市販後副作用報告に関係する内容
【治験】:治験副作用報告に関係する内容
Q&A詳細
| Q36:【市販後】 施行規則第 228 条の 20 第1項第1号ハ(4)の「死亡又は(1)から(3)までに 掲げる症例に準じて重篤である症例」とは、どのように考えたらよいか? | A36:【市販後】 ICHの規定(E2Dガイドライン参照)の「その他の医学的に重要な状態と判断される事象又は反応」すなわち直ちに生命を脅かしたり死や入院に至らなくとも、患者を危機にさらすおそれがあったり、「死に至る」、「永続的又は顕著な障害・機能不全に陥 る」、「生命を脅かす」、「治療のための入院又は入院期間の延長が必要である」ような結果に至らないように処置や治療が必要となるような重要な医学的事象の場合がこれに該当する。例えば、救急処置室等又は自宅において集中治療を必要とするアレルギ ー性気管支痙攣、入院には至らないものの血液障害又は痙攣を来した場合、薬物依存症又は薬物乱用等がこれに該当する。 |
| Q37:【市販後】 施行規則第 228 条の 20 の「後世代における先天性の疾病又は異常」とは、どのように考えたらよいか? | A37:【市販後】 ICHの規定(E2Dガイドライン参照)の「先天異常・先天性欠損を来すもの」に該当し、妊娠前又は妊娠中の医薬品による曝露により出生児に異常を来したと疑われる場 合が該当する。例えば、サリドマイドによる出生児の器官形成不全、ジエチルスチルベストロールによる出生女児の膣癌等が挙げられる。 |
補足:もちろん当局報告として評価判断が必要だが、Special situationの考慮も必要
| Q38:【市販後】 「医薬品等の副作用の重篤度分類基準について」(平成4年6月 29 日付け薬安第 80 号厚生省薬務局安全課長通知。以下「重篤度分類通知」という。)は、重篤性の判断において、どのような位置付けか? | A38:【市販後】 重篤性の判断は、上記のA30の表で示されたICHにおける副作用の重篤性の定義と照らし合わせて行うこと。重篤度分類通知は、あくまでも送信者が症状の程度を判断する上での目安であり、重篤度分類のグレード分類から重篤性を判断するものではない(例えば、グレード3として示されている臨床検査値の変動のみで「重篤」に該当するとは必ずしもいえない)。 |
補足①:上記のA30の表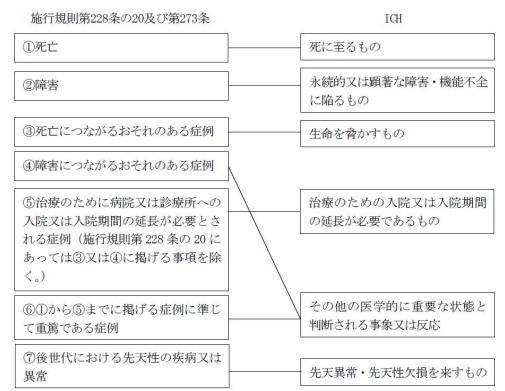
補足②:重篤度分類のグレード分類(以下クリックすると「有害事象共通用語規準 v5.0 日本語訳 JCOG 版」が表示されます)
Common Terminology Criteria for Adverse Events(CTCAE) Version5のGrade分類
(5)記載要領
| Q39:【市販後】 E2B(R3)二課長通知の別紙1及び別紙2中の簡略記載が可能な項目について、これらの項目はどのように記載すべきか? | A39:【市販後】 E.i.1.1a、E.i.1.1b及び E.i.1.2を除き、これらは完了報告の際に必ず記載が必要な項目であり、全く記載しないとエラー報告となるため、例えば、既知・重篤(死亡 症例を除く)の副作用等報告における使用上の注意記載状況等を「J2.11 その他参考 事項等」に記載する場合は、「添付文書に記載済」等の簡略化した表現で差し支えない。 |
補足:「E2B(R3)実装ガイドに対応した市販後副作用等報告及び治験副作用等報告について薬生薬審発 0710 第1号、薬生安発 0710 第1号、令和元 年 7 月 1 0 日」に■簡略記号可能な項目として下線付きで変更前と後で明記されています。外国症例の報告は簡略記号による報告が可能です。
| Q40:【市販後】【治験】 タイムゾーンの記載に当たっての注意事項はあるか? | A40:【市販後】【治験】 日付/時刻の記載方法については E2B(R3)実装ガイド付録 II を参照すること。なお、項目間データチェック等を行う際は、タイムゾーンの記載が無い場合は日本時間 (+09:00)として、タイムゾーンが記載されている場合は日本時間に換算して実施する ので、取扱いには注意すること。 |



コメント